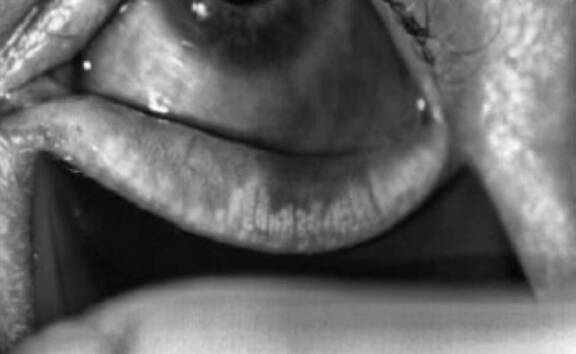
Les dysfonctionnements meibomiens revisités
Les dysfonctionnements des glandes de Meibomius (MGD) sont une cause majeure, peut-être la plus fréquente, de sécheresse oculaire. Ils sont provoqués par la combinaison de différents mécanismes tels que l’évaporation accrue des larmes et l’inflammation de la surface oculaire. Cependant, la physiopathologie et la nosologie de ces mécanismes restent floues, tout comme le rôle joué par les paupières et le film lacrymal, à la fois victime et véhicule de l’inflammation. Différentes causes étant à l’origine de cette pathologie, il est difficile de donner une explication univoque de sa physiopathologie.